Иммунотерапия миом матки
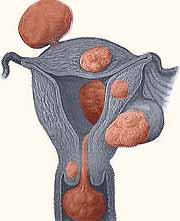 Что такое миома матки и ее симптомы
Что такое миома матки и ее симптомы
Миома матки – одна из самых распространенных опухолей женских половых органов – доброкачественная опухоль, развивающаяся из мышечных и соединительнотканных элементов.
В зависимости от соотношения паренхимы и стромы эта опухоль ранее имела различные названия: миома, фиброма, фибромиома. Однако, принимая во внимание, что узлы миомы чаще развиваются именно из мышечной клетки, большинство авторов считают более правильным термин "миома" ("лейомиома").
Миома матки – наиболее частая опухоль области малого таза и может быть обнаружена примерно у 15-20% женщин репродуктивного возраста [1]. В структуре гинекологических заболеваний она составляет 27%.
Хотя в большинстве случаев миома – медленно растущая опухоль, у 20-40% женщин в возрасте 35 лет и старше миомы достигают значительных размеров и обусловливают выраженную клиническую симптоматику [2]. Кроме того, миома может возникать снова у 7-28% больных, а иногда даже перерождаться в злокачественную опухоль.
Исследования продемонстрировали, что у женщин, родивших по крайней мере двоих детей, риск развития миомы уменьшен наполовину по сравнению с бездетными женщинами. Правда, ученые не уверены, в действительности ли деторождение защищает женщин от возникновения миомы, либо именно миома является фактором бесплодия у не имеющих детей женщин.
Для последующего роста узлов опухоли требуется дальнейшее накопление неблагоприятных факторов, вызывающих опухолевую прогрессию: аборты, длительная неадекватная контрацепция, хронические, подострые и острые воспаления матки и придатков, стрессы, ультрафиолетовое облучение, образование кист и кистом яичников. У женщины, перенесшей к 30 годам 10 абортов, риск образования миомы матки к 40 годам возрастает в 2 раза.
Развитие миомы матки представляет собой доброкачественную контролируемую гормонами диффузную или очаговую гиперплазию миометрия и характеризуется многообразием факторов патогенеза и системных нарушений, хотя причины возникновения миомы до сих пор неизвестны.
Миома матки возникает на фоне гиперэстрогении, прогестерондефицитных состояний, гипергонадотропизма. Большинство исследователей считают, что рост миомы зависит от концентрации цитозольных рецепторов в половых гормонах и сложных механизмов их взаимодействия с эндогенными или экзогенно-вводимыми гормонами. Исходя из клинических наблюдений, можно отметить, что рост и регрессия миомы эстроген-зависимы, так как наблюдается увеличение размеров опухоли во время беременности и уменьшение их после менопаузы [3]. Остается спорным вопрос, является ли уменьшение миоматозных узлов следствием уменьшения количества рецепторов или результатом снижения уровня эстрогенов, прогестерона и андрогенов (существует гипотеза о том, что миомы могут быть чувствительными к андрогенам).
В миоматозных клетках часто обнаруживают хромосомные аномалии (12q13-15) [4]. Действительно, в 30-40% случаев склонность к образованию миомы матки передается по наследству от матери к дочери. Существуют так называемые "семейные формы" миомы матки, когда у всех женщин в семье – бабушки, мамы, тети, сестры – были миомы.
Выявляется миома чаще всего на профосмотре у гинеколога. При этом врач может только констатировать факт наличия миомы матки. В других ситуациях первыми признаками миомы могут быть боли внизу живота или в области поясницы, кровотечения, изменения менструального цикла, нарушение функций соседних органов, например, учащенное мочеиспускание.
Для того чтобы определить количество узлов, их размеры, расположение и т. д., необходимы специальные исследования. Чаще всего достаточно ультразвукового исследования, но иногда врачи для уточнения диагноза могут назначить компьютерную томографию, ядерно-магнитный резонанс.
Миомы могут располагаться в наружном, среднем и внутреннем слоях матки (субсерозные, интерстициальные и субмукозные миомы матки). Узлы могут находиться в теле (95%) и шейке (5%) матки [5]. Наиболее "неприятные" те узлы, которые находятся во внутреннем слое. Такие миомы деформируют полость матки и, как правило, вызывают обильные ежемесячные кровотечения с резким понижением гемоглобина (поэтому при железодефицитной анемии гинекологическое обследование совершенно необходимо).
Современные направления лечения
Само по себе наличие миомы не всегда является показанием к операции. Все зависит от состояния больной, выраженности симптомов заболевания и размеров опухоли.
Показаниями к операции по удалению миомы матки являются боли, быстрый рост размеров узла, подозрение на перерождение миомы матки в злокачественную опухоль, нарушение кровоснабжения в узлах миомы и воспалительные изменения в них, нарушение функций соседних органов (мочевого пузыря, кишечника), бесплодие (когда все другие причины уже исключены). Если опытный гинеколог считает, что операция необходима, то чем раньше она будет сделана, тем лучше.
Миому матки нужно наблюдать в динамике (с использованием ультразвукового исследования влагалищным датчиком), и во многих случаях этого вполне достаточно, а никакого лечения – ни консервативного, ни тем более оперативного – не требуется. Если женщина периодически испытывает дискомфорт или боли в области малого таза, эффективен прием нестероидных противовоспалительных препаратов. При наличии клинической симптоматики можно проводить консервативную терапию препаратами гестагенов (норколут, дуфастон, премалют, медроксипрогестеронацетат), агонистов гонадотропин-рилизинг гормонов (золадекс). Транексамовая кислота в таблетках может уменьшить степень кровотечения. Этим же свойством обладают противозачаточные таблетки. Прием даназола, обладающего андрогенными свойствами, способствует уменьшению размеров миомы, но вызывает неприятные побочные эффекты: огрубение голоса и гирсутизм. Более эффективны гормоны, вызывающие искусственную менопаузу, такие как бузерелин (применяемый в виде назального спрея) и гозерелин (ежемесячно вводимый в виде инъекций. Следует учитывать, что гормональное лечение способно только на время облегчить состояние больных миомой матки, в то же время являясь причиной тяжелых побочных эффектов. Например, длительная гипоэстрогенемия сопровождается риском остеопороза [1, 6], а после отмены гормональных препаратов рост миом ускоряется (у 20% женщин рецидивирование наступает в течение 12 месяцев, а у 50% – в течение 5 лет) [4]. Назначение гормональных препаратов ради того, чтобы уменьшить размер узла, совершенно неоправданно.
Еще одна цель гормональной терапии заключается в снижении величины кровопотери и продолжительности оперативного вмешательства при консервативной миомэктомии (удалении миоматозного узла или узлов) или гистерэктомии (удалении матки).
Консервативную (лапароскопическую) миомэктомию производят до 40 лет при наличии показаний к хирургическому лечению. Особенно целесообразно удалять макроскопические миоматозные узлы средних размеров (в диаметре от 2 до 5 см), пока не произошло их интенсивное увеличение. При решении вопроса о консервативной миомэктомии необходимо принимать во внимание морфотип опухоли. При пролиферирующей миоме можно удалить несколько узлов, но дальнейший рост продолжают множество других зачатков роста. Поэтому рецидивы при консервативной миомэктомии при миоме матки имеют место в 15–37% случаев. Следует также учитывать, что это оперативное вмешательство все же сопровождается стандартным хирургическим риском, не исключая возможности развития тяжелых осложнений.
В настоящее время разработан еще один малоинвазивный метод лечения – чрезкатетерная эмболизация миоматозных узлов, при котором узел лишается кровоснабжения и подвергается регрессу без малейшего вреда для матки в целом, но этот метод все еще остается экспериментальным и широко не применяется [7]. Проводятся исследования результатов эмболизации в отношении фертильности и рецидивирования узлов.
После 40 лет и в постменопаузальном возрасте при наличии хирургических показаний необходима операция удаления миоматозной матки, т.к. если миома не регрессировала в первые 2 года постменопаузы, дальнейшее ее существование сопровождается опасностью возникновения онкопатологии (аденокарцинома, саркома).
Иммунотерапия вакциной РЕСАН
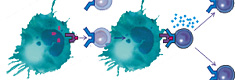
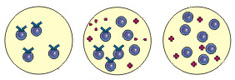
Прогрессирующее развитие миоматозного узла или, иными словами, его истинный рост, можно остановить, блокируя размножение миогенных элементов периферической зоны узла, в то же время стимулируя процессы апоптоза миоцитов в центральных отделах узла. Отнюдь не все лекарственные препараты, которые применяются сейчас при лечении миомы матки и действительно оказывающие лечебное воздействие на симптомы, сопровождающие ее развитие, обладают подобным действием. Методы иммунокоррекции как раз реализуют эти эффекты. Восстановление иммунной реактивности, иммунокоррегирующая терапия, требует специальных подходов стимуляции системы иммунитета. Разработано совершенно новое направление лечения эндометриоза – иммунотерапия с использованием противоопухолевой вакцины РЕСАН, которая способствует формированию специфического иммунного ответа против этого заболевания [9, 10].
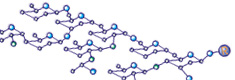
Компоненты системы иммунитета распознают определенные поверхностные антигены клеток ткани. Важную роль при этом играет относительное содержание на клеточной поверхности молекул клеточной адгезии различных классов, главным образом Е-катгеринов [11, 12, 13, 14] и опухольассоциированных антигенов CA125, СA19-9, CA15-3. Хотя митотическая активность миом матки, как правило, низкая, клетки миомы экспрессируют онкобелки пролиферации (Ki–67) и онкобелки, снижающие процесс апоптоза (bcl–2, bax).
По этим причинам мы рекомендуем применение имитаторов опухолевых антигенов, входящих в состав вакцины РЕСАН, с целью коррекции системы иммунитета для лечения больных фибромиоматозом [10].
Показания к иммунотерапии вакциной РЕСАН:
- Молодой возраст пациентки (репродуктивный и пременопаузальный).
- Небольшие размеры миоматозно измененной матки (до 10–12 недель беременности).
- Межмышечное расположение миоматозных узлов.
- Относительно медленный рост миомы.
- Отсутствие деформации полости матки (т.е. центрипетального роста и подслизистой локализации).
В какой-то степени мы можем провести аналогию между показаниями к лечению вакциной РЕСАН и показаниями к органосохраняющим оперативным вмешательствам при полной безопасности применения вакцины.
Ниже приводиться сокращенный вариант протокола применения вакцины РЕСАН у женщин с различной генитальной патологией.
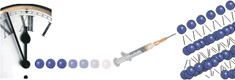
Мы наблюдали 35 женщин, среди которых были 12 больных, страдающих генитальным эндометриозом – аденомиозом, позадишеечными формами эндометриоза, наружным генитальным эндометриозом, 13 больных миомой матки, 10 больных – с сочетанными формами эндометриоза и миомы матки; у двух пациенток имелись кистозные образования яичников [8]. У всех пациенток наблюдались дисгормональные гиперплазии молочных желез. Ранее больные получали различное лечение, включающее гормонотерапию, курсы иммуномодуляторов, антиоксидантную терапию. Однако эффект от полученного медикаментозного лечения не был длительным, сроки ремиссии ограничивались 2-3 месяцами после окончания приема препаратов, причём улучшение касалось в основном клинической симптоматики (некоторое уменьшение болевого синдрома, незначительное улучшение общего состояния). В связи с кратковременным и недостаточно выраженным эффектом от предыдущей медикаментозной терапии мы проводили пациенткам курс иммунотерапии ксеногенной вакциной, которая имитировала эндометриозные и миомные антигены [10]. Всем наблюдаемым больным инъекции вакцины производились внутрикожно однократно.
Больные были обследованы до и после лечения. Болевой синдром оценивали по Mac Laverty:
боли в области таза, не связанные с половым актом или менструацией (3 балла – интенсивные, резкие, почти постоянные, больные были вынуждены принимать анальгетики; 2 балла – умеренные, терпимые, заметный дискомфорт в течение большей части цикла; 1 – слабые, временами ощущение дискомфорта или боли перед менструацией);
альгодисменорея (3 балла – сильная, заставляет больную оставаться в постели целый день или несколько дней; 2 балла – умеренная заставляет больную оставаться в постели несколько часов в день, временами – нетрудоспособность; 1 балл – слабая, с некоторым нарушением трудоспособностии);
диспареуния – боль во время полового сношения (3 балла – настолько сильная, что вынуждает избегать сношений; 2 балла – умеренная, что вынуждает прервать сношение; 1 балл – имеется, но терпимая);
дисменорея (3 балла - кровомазание до менструации от 4-х до 7 дней; 2 балла – от 1 до 3 дней; 1 балл – периодически появляющиеся кровомазания до менструации);
выраженность менструаций (3 балла – обильные, 2 балла – умеренные менструации, 1 балл – скудные менструации).
Проводили бимануальное исследование, УЗИ гениталий и молочных желез, маммографию. Исследование крови для определения уровней опухолевых маркеров (CEA, СА-125, СA19-9, СА-15-3), антигенов вируса гепатита В, титров антител к антигенам Сhlamydia trachomatis, Toxoplasma gondii, Mycobacterium tuberculosis и вируса гепатита С проводили методом иммуноферментного анализа. Использовали фотометр STAT FAX 303 PLUS, автоматические дозаторы BIOHIT и реактивы фирм HOFFMANN-LA-ROCHE, HUMAN, BCM DIAGNOSTICS LLC, LABODIA-XЕМА, ВЕКТОР-БЕСТ, в системе GLP.
До лечения болевой синдром в 9 баллов был у 27 человек, страдающих генитальным эндометриозом и сочетанными формами эндометриоза и миомы матки. У 8 больных миомой матки болевой синдром не превышал 5 баллов. Дисменорея оценивалась 3 баллами у всех больных генитальным эндометриозом и сочетанными формами эндометриоза и миомы матки, у пациенток с миомой матки (13 человек) – 1 балл.
При бимануальном исследовании и УЗИ гениталий у всех пациенток в той или иной степени определялась неоднородность консистенции миометрия, перемежающиеся участки уплотнений и тестоватости в толще матки, увеличение размеров матки, в области перешейка отмечалась умеренно выраженная пастозность, резкая болезненность. При УЗИ гениталий у всех наблюдаемых 12 больных генитальным эндометриозом выявлены признаки аденомиоза матки 3 и 4 степени. У пациенток с сочетанными формами эндометриоза и миомы матки определялись на фоне неоднородной мозаичной структуры интерстициальные, субсерозные и субмукозные (у 5 больных) узлы диаметром от 22 до 33 мм, дающие акустическую дорожку. Размеры матки во всех наблюдениях были увеличены до 9-16 недель.
При УЗИ молочных желез у всех пациенток обнаруживались изменения, характерные для диффузной (23 больных) и фиброкистозной (12 человек) мастопатии. Данные УЗИ молочных желез совпадали с данными маммографии.
Показатели опухолевых маркеров были повышены до лечения у всех пациенток, но не превышали границ доброкачественности. Средние значения СА-125 в целом в группе составили: 44,7+-1,34 МЕ/мл, СА-19-9 28,9+-1,5 Ед/мл, СA-15-3 53,2+-4,3 Ед/мл, CEA 1,29+-0,38 нг/мл.
По наличию инфекции наблюдаемые больные распределились следующим образом: носительство вирусов гепатитов В и С – 27 человек (из 35), Chlamydia trachomatis – 18, Toxoplasma gondii – 12, Micobacterium tuberculosis – 6 пациенток. Важно, что клиническое состояние больных и уровни антител, маркеров данных инфекций, указывали на хроническую персистенцию инфекции и отсутствие обострений. Наличие этой инфекции влияло на самочувствие ряда больных после вакцинации. В течение 7-10 дней после вакцинации 30 больных беспокоили слабость, у больных хламидиозом отмечались боли в суставах. Некоторая тошнота и незначительное ухудшение общего состояния на фоне вакцинации наблюдалась у носителей вирусов гепатитов. Носители туберкулезной и токсоплазменной инфекции практически не имели клинических признаков обострений, за исключением 2 пациенток, у которых в течение 1-1,5 месяцев после вакцинации мы наблюдали вялотекущее обострение хронического бронхита. Затем состояние больных стабилизировалось, и никаких побочных явлений в течение последующих 3-4 недель наблюдения пациентки не отмечали. В сыворотке крови мы отмечали тенденцию к росту титров антител к указанным инфекциям, с последующим снижением в течение 1,5 – 2-х месяцев до первоначального уровня.
Через 1 месяц после проведенной вакцинации были повторно обследованы все больные. При бимануальном исследовании у пациенток, страдающих эндометриозом, значительно уменьшились размеры матки, консистенция миометрия чаще была однородной или с небольшими участками уплотнений. При наличии миомы матки с узлами различных размеров наблюдалось уменьшение узлов и тела матки. При генитальном эндометриозе все благоприятные сдвиги были выражены ещё значительнее. У всех наблюдаемых больных эндометриозом УЗИ гениталий выявило уменьшение размеров матки и очагов генитального эндометриоза, у пациенток с сочетанными формами эндометриоза и миомы матки определялось уменьшение размеров интерстициальных, субсерозных и субмукозных узлов диаметром от 16 до 26 мм. Размеры матки во всех наблюдениях уменьшились до 5-11 недель (Рис.1).

Рис. 1. Размер матки
У 7-ми пациенток наблюдалась нормализация размеров матки, у этих же пациенток при УЗИ подтверждено полное исчезновение миоматозных узлов. У 2-х пациенток, имевших кистозные образования яичников, мы наблюдали их полное исчезновение (размеры рассосавшихся кист составили от 14,5 см3 до 26,4 см3).
При УЗИ молочных желез у всех пациенток с диффузной мастопатией уже через один месяц после введения вакцины никаких патологических изменений тканей молочной железы не определялось. При фиброзно-кистозной форме мастопатии очаги кистозных изменений уменьшились в размерах на 1,5-3 мм. Данные УЗИ молочных желез совпадали с показателями маммографии.
Болевой синдром у 22 человек, страдающих генитальным эндометриозом и сочетанными формами эндометриоза и миомы матки, снизился до 5-7 баллов (Рис. 2).

Рис. 2. Выраженность болевого синдрома
После вакцинации дисменорея оценивалась 1 баллом у всех больных эндометриозом и сочетанными формами эндометриоза и миомы матки, у пациенток с миомой матки (13 человек) дисменорея составила 0 баллов (Рис. 3).

Рис. 3. Дисменорея
Ни в одном из случаев мы не наблюдали клинического ухудшения. Больные отмечали уменьшение отеков, исчезновение болевых ощущений в области эстрогензависимых органов, общее улучшение самочувствия, повышение настроения.

Рис. 4. Изменение уровней опухолевых маркеров
Изменение уровней опухолевых маркеров было различным в зависимости от вида маркера (Рис. 4). Так, уровни СA-19-9 после вакцинации повышались в среднем на 23% (P < 0,1%) от первоначального уровня в течение месяца, через 2 месяца они были меньше первоначального на 15%. Уровни СA-125 в среднем равномерно снижались до 25% (P < 0,1%) от исходного, у одной пациентки мы наблюдали повышение уровня СА-125 на 14% от исходного уровня в течение первого месяца после вакцинации с последующим снижением на 25% ниже исходного через 2 месяца от момента вакцинации, данная пациентка отличалась от остальных более глубоким расположением миоматозного узла в матке. Уровни СA-15-3 снижались на 38% (P < 0,1%) от первоначального уровня уже в течение первого месяца после вакцинации. Средние значения СA-15-3 через 2 месяца после вакцинации составили 31,0 Ед/мл (P < 0,1%). Изменения этих показателей указывают на положительную динамику и эффективность данной иммунотерапии.
Таким образом, при сопоставлении полученных результатов выявлено, что применение вакцины РЕСАН вызывает значительное улучшение состояния больных и показателей объективного исследования у всех наблюдаемых пациенток. Мы рекомендуем обследование больных перед вакцинацией на наличие хламидийной, туберкулезной инфекции, а также на носительство вирусов гепатитов В и С. В случае обнаружения высоких титров антител к указанным инфекциям необходимо провести предварительную санацию организма (антибиотиками, интерферонами, интерлейкинами) с последующей вакцинацией.
Иммунотерапия ксеногенной вакциой РЕСАН миом матки и их сочетанных форм с эндометриозом приводит к регрессии или полному исчезновению миоматозных узлов, очагов эндометриоза и кистозных образований яичников.
Информационные источники
1.Article: Uterine fibroids. Review Date: 04/09/01 Reviewed By: Catherine S. Bradley, M.D., Department of Obstetrics and Gynecology, University of Pennsylvania Medical Center, Philadelphia, PA.
2.An Alternative To Hysterectomy. Интерактивно.
3.Сметник В. П. // Пробл. репродукции. - 1995. - # 2.- С. 8 - 14
4.Uterine Myomata Fibroid Tumors 1998-2001 T. J. Clark & Company. Интерактивно.
5.Большой Медицинский Сайт. Миома матки. Интерактивно.
6.Fibroids and Estrogen Therapy. Интерактивно.
7.New Treatment for Uterine Fibroids Avoids Surgery. Edward L. Siegel, MD, Department of Radiology, University of Kansas Medical Center. Интерактивно.
8.The vaccinotherapy of patients with mastopathy, endometrios and mioma of uterus A. Ovsienko, H. Doronina, V. Yanchenko Journal of Immunopathology: http://iaci.ru/journal/
http://iaci.ru/journal/issue2/full_text/sec6ar2.pdf
9.Novikov D.K., Novikiva V. I., Derkatch U.N., Novikov P.D. The basic immune corrections. Vitebsk, 1998, pg. 106.
10.Yantchenko V.V., Yantchenko A.V., Yantchenko L. K. Immitators of the tumor antigens. The patent committee RB, appl. N970547, 1997.
11.Gaetje R. Kuteian S., Herrmann G. Invasiveness of endometriotic cells in vivo. // Lancet, 1 995, V346, P 463-1 464.
12.Gamallo C., Palacios J., Suarez A. Correlation of E-cadherin expression with differentiation grade and histological type in breast carcinoma. // Am. J. Pathol., 1 993, V 42, P987-993.
13.Inoue M., Ogawa F., Miyata M. Expression of E-cadherin in normal, benign, and malignant tissues of female genital organs. // Am. J. Clin. Pathol., 1 992, V98, P76-80.
14.Jimbo H., Hitomi Y., Yoshikawa F. Evidence for monoclonal expansion of epithelial cells in ovarian endometrial cyst. // Am. J. Pathol., 1 997, V 50, P 73-11 78
15.Союнов М. А. Клиника, диагностика и лечение узловатой формы аденомиоза. // Акушерство и гинекология. – 1987. - № 3. – С. 34-36.
16.Лопухов Д. А. Клинико-диагностическая характеристика сочетанной доброкачественной патологии матки в перименопаузе: Автореферат дис. …канд. Мед. Наук: 14.00.01. – М., 1992. – 33 с.
17.Новые данные о патогенезе внутреннего эндометриоза. / М. М. Дамиров, В. И Кулаков, Л. П. Бакулева и др. // Акушерство и гинекология. – 1993. № 5. – С. 28-32.
18.Ferenczy A. Pathophysiology of adenomyosis. // Hum. Reprod. Update. - 1998. - Vol. 4, № 4. – P. 312-322.